Voer een woord of zin in in een taal naar keuze 👆
Taal:
Vertaling en analyse van woorden door kunstmatige intelligentie
Op deze pagina kunt u een gedetailleerde analyse krijgen van een woord of zin, geproduceerd met behulp van de beste kunstmatige intelligentietechnologie tot nu toe:
- hoe het woord wordt gebruikt
- gebruiksfrequentie
- het wordt vaker gebruikt in mondelinge of schriftelijke toespraken
- opties voor woordvertaling
- Gebruiksvoorbeelden (meerdere zinnen met vertaling)
- etymologie
Wat (wie) is Азота окислы - definitie
Оксид азота; E918; Е918; Окислы азота; Азота оксиды; Кислородные соединения азота
Азота окислы
соединения азота с кислородом. Известны N2O, NO, N2O3, NO2 (и его димер N2O4), N2O5; есть сведения о существовании NO3, не выделенного в свободном состоянии. При высокой температуре в пламени вольтовой дуги, а в природе - при электроразряде из смеси азота с кислородом образуется окись азота NO, которая при охлаждении переходит в NO2. Другие А. о. получают косвенным путём. N2O5 - твёрдое вещество; остальные окислы при обычных условиях газообразны.
Закись азота N2O - бесцветный газ со слабым приятным запахом и сладковатым вкусом; вдыхание смеси воздуха с N2O вызывает состояние, напоминающее опьянение (отсюда название - веселящий газ). Плотность при 0°С и 101 325 н/м2 (760 мм рт. ст.) 1,9804 кг/м3, tкип - 89,5°С, tпл - 102,4°С. 1 объём N2O при 5°C растворяет 1,048 объёма N2O. Химически N2O с водой, растворами кислот и щелочей не реагирует, кислородом не окисляется. Выше 500°C разлагается: 2N2O = 2N2 + O2; поэтому при повышенных температурах действует как сильный окислитель и поддерживает горение. Получают N2O термическим разложением нитрата аммония: NH4NO3=N2O+ 2H2O. В медицине служит для общей анестезии.
Окись азота NO - бесцветный газ, буреющий при соприкосновении с воздухом вследствие окисления до NO2. Плотность при 0°С и 101 325 н/м2 (760 мм рт ст) 1,3402 кг/м3, tкип-151,8°С, tпл-163,6°С. В воде мало растворима (0,0738 объёма в 1 объёме H2O при 0°С). С водой, кислотами и щелочами химически не взаимодействует. Образует многочисленные продукты присоединения, например нитрозилхлорид NOCI. Получают NO действием разбавленной азотной кислоты на некоторые металлы, например: 3Cu + 8HNO3= 3Cu(NO3)2 + 4H2O + 2NO. Окись азота - важный полупродукт окисления аммиака при получении азотной кислоты (См. Азотная кислота).
Азотистый ангидрид (трёхокись азота) N2O3 - в обычных условиях неустойчивое соединение. Разлагается уже при 0°С:
Около 3,5°С кипит с разложением, при 25°C содержит только 10\% недиссоциированного N2O3. При низкой температуре может быть получен в виде тёмно-голубой жидкости, при сильном охлаждении - светло-голубой массы с tпл -102°С. С водой образует азотистую кислоту (См. Азотистая кислота): N2O3 + H2O = 2HNO2, со щелочами - соли (см. Нитриты). N2O3 получают по реакции: N2O4+ 2NO = 2N2O3; практического применения не находит.
Двуокись азота NO2 - бурый газ с удушливым запахом, при 21,15°C - буро-красная жидкость, бледнеющая при дальнейшем охлаждении из-за образования четырёхокиси азота N2O4 , tотв -11,2°С. Взаимодействует с водой с образованием азотной кислоты и окиси азота: 3NO2 + H2O = 2HNO3 + NO; со щелочами образует нитраты и нитриты. Двуокись азота - сильный окислитель; в токе NO2 энергично сгорают уголь, сера, фосфор, органические соединения. В промышленности NO2 получают окислением NO при производстве азотной кислоты, в лаборатории - термическим разложением некоторых нитратов: 2Pb(NO3)2 = 2PbO + O2 + 4NO2. Применяют NO2 как нитрующий агент (см. Нитрование органических соединений).
Азотный ангидрид (пятиокись азота) N2O5 - бесцветные очень летучие кристаллы. Крайне неустойчив и взрывоопасен. Взаимодействует с водой, давая азотную кислоту: N2O5 +Н2O = 2HNO3, со щелочами образует соли - Нитраты. В лаборатории получают по реакции: 2HNO3 + P2O5 = N2O5+ 2HPO3. Практического применения не находит. Все А. о. физиологически активны.
Лит. см. при ст. Азот, Азотная кислота.
Фториды азота
СТРАНИЦА ЗНАЧЕНИЙ В ПРОЕКТЕ ВИКИМЕДИА
Азота фториды
неорганические соединения, содержащие связь N-F, например трифторид азота NF3, тетрафторгидразин N2F4, дифторамин NF2H, фтористый нитрозил FNO и др. Ф. а. - бесцветные газы со специфическим запахом. При нагревании разлагаются на элементы или трифторид азота и азот (за исключением NF3 и FNO). Проявляют свойства сильных окислителей. С органическими соединениями некоторые Ф. а. образуют многочисленные органические вещества, содержащие группы -NF2 и -NONF. Особенность Ф. а. состоит в том, что при взаимодействии с сильными льюисовскими кислотами (см. Кислоты и основания) они образуют соли с фторазотными катионами 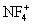 ,
, 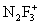 ,
, 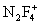 , F2NO+.
, F2NO+.
Трифторид азота, NF3 - газ; tпл - 208,5°С, tkип - 129,1°С. Окислительная способность проявляется при высоких температурах. Превращается в тетрафторгидразин при повышенных температурах и в присутствии меди, железа, ртути или угля. Получается электролизом расплава дифторида аммония или фторированием азотсодержащих веществ. Применяется в производстве тетрафторгидразина.
Тетрафторгидразин, N2F4 - газ; tпл - 161,5°С, tkип - 74,2°С. Способен к диссоциации: N2F4 ⇔ 2NF2. При 150°С и давлении 0,1 Мн/м2 (1 кгс/см2) степень диссоциации 0,2. Диссоциация N2F4 обусловливает его дифтораминирующее действие, которое проявляется, например, в присоединении к олефинам:
. Тетрафторгидразин получается конверсией трифторида азота над углём (промышленный метод), разложением NF2H или окислением его растворов. Применяется для синтеза органических дифтораминосоединений.
Дифторамин, NF2H - газ; tпл - 116°С, tkип - 23°С. Взрывается при ударе (особенно в жидком и твёрдом состояниях). Проявляет амфотерные свойства. В реакциях действует как дифтораминирующий агент. Получается действием серной кислоты на дифтораминомочевину (продукт фторирования мочевины) или на трифенилметил дифторамин, синтезируемый из N2F4 и трифенилметилхлорида в присутствии ртути. Применяется для синтеза органических дифтораминосоединений.
Лит.: Панкратов А. В., Химия фторидов азота, М., 1973.
А. В. Панкратов.
Фториды азота
СТРАНИЦА ЗНАЧЕНИЙ В ПРОЕКТЕ ВИКИМЕДИА
Азота фториды
Фториды азота — неорганические соединения азота со фтором. Известны трифторид азота NF, Дифтордиазин NF, тетрафторгидразин NF, азид фтора FN, а также оксифторид азота NOF.
Wikipedia
Оксиды азота
Окси́ды азо́та — неорганические бинарные соединения азота с кислородом.
Voorbeelden uit tekstcorpus voor Азота окислы
1. Здесь прекрасно понимают: никакие фильтры, о которых твердят на заводе, не в состоянии удержать оксиды азота и углерода, диоксиды азота, окислы кремния и прочих "летучих голландцев", сопровождающих производство керамического кирпича.
